Capítulo 2, "Controlando a Magia da Biologia"
Os cientistas que estudam as Ciências da Vida anseiam por compreender o mundo natural. Persistentemente, tentam desvendar os mistérios da biologia, porque estes mistérios são inerentemente intrigantes. Mas, mais urgentemente, os cientistas querem compreender como funcionam os sistemas biológicos, para conseguir controlá-los. Este controlo traz inúmeros e importantes benefícios para a saúde e para a economia humana. O controlo da magia da biologia tem subjacente a extraordinária promessa da biotecnologia.
É Biologia, É Química… É Engenharia!
Isto é, engenharia metabólica. Nesta área entusiasmante, a biologia e a química andam de mãos dadas. O objetivo consiste em utilizar as ferramentas da biologia para produzir compostos químicos que, em muitos casos, nunca existiram na natureza: produtos naturais "não naturais". Os engenheiros metabólicos utilizam sistemas vivos para transformar açúcares simples e outras pequenas moléculas em novos e promissores antibióticos — mesmo produtos agrícolas e veterinários.
Alguns engenheiros metabólicos não são sequer engenheiros, mas sim biólogos que desenvolveram o necessário conhecimento de química, ou químicos que aprenderam a biologia de que precisavam. Muitos engenheiros metabólicos são, na realidade, engenheiros pela prática. Seja qual for a sua formação, todos os engenheiros metabólicos olham para o metabolismo de uma forma pouco convencional. Estes cientistas vêm as vias metabólicas como mini laboratórios de química, capazes de empreender reações químicas múltiplas num único recipiente — a célula — dispensando demorados e trabalhosos procedimentos de separação e purificação.
Os engenheiros metabólicos fazem os seus passes de magia alterando o metabolismo de uma célula bacteriana, vegetal ou animal. Para alcançar este objetivo, os investigadores têm que isolar primeiro as vias bioquímicas que estes organismos normalmente usam para degradar alimentos, produzindo energia (o que se designa por vias catabólicas), assim como aquelas vias que reutilizam as unidades estruturais para produzir moléculas de maiores dimensões (o que se designa por vias anabólicas. As vias metabólicas são as que estão envolvidas na síntese ou na degradação de moléculas apropriadamente designadas por metabolitos.
Atualmente, mais de uma centena de metabolitos estão na base de medicamentos para humanos, assim como para animais. Os antibióticos eritromicina e tetraciclina, um medicamento para baixar o colesterol denominado lovastatina (Mevacor®), e um desparasitante antipulgas denominado avermectina são todos policetídeos, uma classe de metabolitos que as bactérias do solo produzem natural e abundantemente. Uma vez que os policetídeos são produzidos em reações em cadeia envolvendo muitas enzimas, os engenheiros metabólicos realizam experiências em que se combinam e reorganizam os genes que codificam estas enzimas para, intencionalmente, alterar o produto final da sequência de reações. Deste modo, podem obter moléculas totalmente novas. Nesta perspetiva, constituíram-se empresas que exploram a natureza em busca dos segredos escondidos que possam permitir aos microrganismos produzir medicamentos mais poderosos e com menos efeitos secundários do que os que estão atualmente em uso. Dado que estes métodos dependem profundamente da biologia, são em muitos casos, consideravelmente menos tóxicos do que os métodos tradicionais de produção comercial, que frequentemente requerem a utilização de químicos potencialmente nocivos para otimizar compostos sintéticos.
As Fábricas Metabólicas Fazem Muito a Partir de Muito Pouco
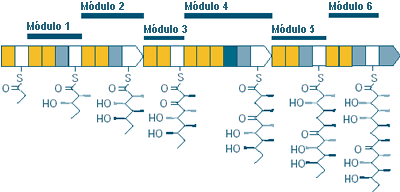
Adaptado com autorização de Kosan Biosciences.
Determinados tipos de bactérias do solo produzem o antibiótico eritromicina — uma estrutura química complexa que contém 37 átomos de carbono, 13 átomos de oxigénio, 67 átomos de hidrogénio e um único átomo de azoto — unicamente a partir de algumas matérias-primas pequenas e simples. As bactérias produzem este antibiótico, amplamente utilizado, através de uma via que consiste numa série de "módulos" enzimáticos, ou mini-fábricas, cada um dos quais é, por sua vez, constituído por, pelo menos, três enzimas distintas. No caso da produção de eritromicina, a função de cada módulo consiste na adição progressiva de dois átomos de carbono à cadeia de átomos em formação que dará origem à eritromicina.
Combinações, Combinações
As companhias farmacêuticas, pequenas ou grandes, dedicam-se à pesquisa de novos compostos, denominados princípios ativos, a fim de testar a sua utilidade no tratamento de doenças. De uma maneira geral, o processo de descoberta de um medicamento envolve dois procedimentos sequenciais: descoberta do princípio ativo e otimização do princípio ativo. Uma metodologia a que as companhias farmacêuticas frequentemente recorrem para descobrir potenciais medicamentos é a química combinatória, um processo em que os químicos criam e de seguida selecionam coleções imensas de compostos ("bibliotecas"). Estas bibliotecas consistem numa compilação diversificada e aleatória de milhares de moléculas distintas, elaboradas a partir de algumas unidades estruturais químicas. Ainda que estas abordagens possam criar um número espantoso de possibilidades, as moléculas constituintes do princípio ativo que são identificadas, através de uma estratégia deste tipo podem necessitar de extenso aperfeiçoamento laboratorial, de modo a transformá-las em moléculas não nocivas para o organismo e que funcionam bem como medicamentos.
Infinitas Possibilidades
Um grande desafio na pesquisa de novos medicamentos é a procura por entre resmas de possibilidades — encontrar uma agulha num palheiro. Um grande número de novas moléculas pode ser produzido por diversos métodos, mas a dificuldade reside em encontrar os adequados. Uma abordagem promissora adotada pelos químicos para o desenvolvimento de potenciais novos medicamentos é a química combinatória, uma técnica do tipo "encontra a agulha", com a qual os químicos criam números de cortar a respiração (milhões) de compostos, a cada um dos quais ligam uma minúscula esfera de plástico. O resultado é uma coleção extensa, ou uma biblioteca, de muitas esferas, cada uma ligada a uma molécula específica. Assim, cada esfera está associada a um medicamento potencialmente bom – uma agulha num enorme palheiro de possibilidades. Os cientistas têm que ser criativos em encontrar meios que permitam distinguir moléculas que, embora semelhantes podem atuar de formas muito diferentes. Por isso os químicos recorrem frequentemente a um código de cores – a melhor molécula mostra-se ao tornar-se, por exemplo, vermelha ou azul, quando analisada através de um sistema químico de deteção do medicamento marcado.
Os Microrganismos Ficam Azuis

Absorto no seu laboratório de microbiologia a estudar como é que a bactéria Escherichia coli (E. coli I, um microrganismo muito comum) degrada substâncias químicas designadas hidrocarbonetos, David Gibson da University of Texas at Austin verificou algo surpreendente: algumas das colónias bacterianas na sua placa de petri tinham desenvolvido uma coloração azul brilhante. Analisando os seus registos, Gibson percebeu que aqueles indivíduos em particular eram precisamente os que ele tinha transformado com um novo gene — que codificava a enzima tolueno dioxigenase. Analisou cuidadosamente o pigmento azul produzido pela nova estirpe bacteriana e deduziu que a coloração foi produzida quando a enzima converteu um simples nutriente denominado indol em índigo, o corante mais vendido mundialmente e que serve para tingir de azul as calças de ganga. Por coincidência, estava-se em 1983, exatamente 100 anos após os químicos do século IXX terem desenvolvido um método de sintetizar quimicamente o corante, mas que se baseia na utilização de matérias-primas nocivas (por exemplo, cianeto) e que também produz subprodutos tóxicos. Cientistas da Amgen, uma empresa em Thousand Oaks, California descobriram que uma enzima muito semelhante, designada por naftaleno dioxigenase, também converte indol em índigo. A Genecor International de Palo Alto, California tentou introduzir o método biológico no mercado índigo de 200 milhões de dólares, mas deparou-se com problemas. Apesar de a produção de índigo por bactérias ser uma inovação biotecnológica amiga do meio ambiente, a síntese química daquele corante é aparentemente muito menos dispendiosa, o que inviabiliza os esquemas comerciais de produção biológica de índigo.
Química Para Um Mundo Mais Verde!
Para além das estratégias de engenharia metabólica, bastante promissoras no que respeita à criação de novos medicamentos, outras áreas da química pretendem fazer a limpeza da Terra, melhorando a saúde humana através da eliminação da poluição do ar e das águas.
Terrence Collins da Carnegie Mellon University, Pittsburgh, desenvolveu uma classe de moléculas, denominada catalisadores, de oxidação, que diminuem a quantidade de cloro necessário a processos de branqueamento industrial. Os catalisadores, obtidos a partir de componentes não tóxicos, podem ser utilizados nas indústrias de papel e de lavandaria e também poderão, um dia, ser utilizados no tratamento de água potável, no que se refere à eliminação de parasitas. Os catalisadores de Collins funcionam induzindo um agente branqueador natural (peróxido de hidrogénio) que ou está presente, ou pode ser facilmente adicionado, a soluções aquosas. Uma vantagem adicional destes catalisadores verdes decorre da possibilidade de pré-determinar o seu prazo de validade. Esta característica, a que Collins chama "marcar-um-tempo-de-vida" permite aos cientistas controlar a durabilidade do catalisador até à sua autodestruição.
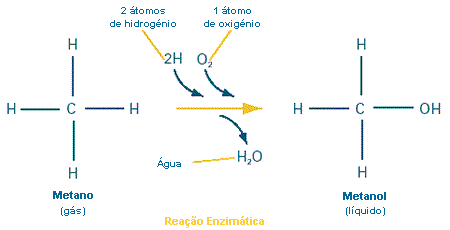
Estratégias químicas inovadoras podem ajudar a reduzir a poluição resultante de processos de fabrico, mas também podem auxiliar na resolução de alguns problemas ambientais que já ocorreram. Para os químicos, a degradação de moléculas pequenas, persistentes e inertes como o metano — um único átomo de carbono rodeado por quatro átomos de hidrogénio — é um desafio técnico. Mas, para uma determinada variedade de bactérias que colonizam fontes termais em Bath, na Inglaterra, a eliminação de metano é muito simples. Como estagiários em miniatura, as bactérias das fontes termais podem oferecer um valioso serviço aos cientistas que trabalham para eliminar o metano do ar, que é o segundo maior contribuinte, a seguir ao dióxido de carbono, para o "efeito de estufa", que tem sido identificado como uma causa do aquecimento global. Nos Estados Unidos, as fontes mais importantes de metano são os aterros e o estrume produzido pelo gado.
Investigadores em biotecnologia adorariam ser capazes de utilizar catalisadores biológicos inofensivos para o ambiente para converter metano em metanol. O químico Stephen Lippard do Massachusetts Institute of Technology, Cambridge, contribuiu com importantes avanços nesta área ao estudar intensivamente as bactérias de fontes termais com a finalidade de identificar o ingrediente mágico — uma enzima — que elas utilizam para eliminar o metano.
Lippard e os seus colaboradores descobriram a estrutura desta enzima, denominada metano monooxigenase (MMO), e o seu modo de funcionamento. Ao que parece, a MMO é uma máquina molecular curiosamente complexa constituída por três componentes distintos. Juntos, os três componentes são capazes de transformar a pequena molécula de metano em metanol, numa reação com oxigénio que substitui um átomo de hidrogénio do metano por um átomo de oxigénio e um de hidrogénio. Esta reação química produz metanol, com água como subproduto (ver figura acima). O facto de uma enzima bacteriana ter esta capacidade é importante. Enquanto que a degradação do metano em laboratório é bastante difícil, o seu primo químico metanol pode ser processado com relativa facilidade. Para além disso, o metanol (um líquido) pode ser transportado muito mais facilmente do que o metano, que é um gás mais difícil de conter.
Acelerando
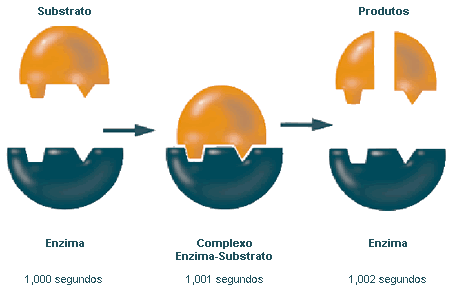
Todas as reações químicas envolvem a conversão de matérias-primas (designadas por substratos) em produtos. Os catalisadores são moléculas que permitem que a reação ocorra mais rapidamente do que ocorreria na sua ausência. Por definição, os catalisadores são facilitadores — não são gastos na reação e podem ser reutilizados. Nas reações industriais — por exemplo, na produção de amónia — os catalisadores podem ser uma mistura de moléculas simples, como o ferro, o potássio, o oxigénio e o alumínio. Os catalisadores do teu organismo são enzimas. Algumas enzimas fazem com que as reações no teu organismo ocorram um bilião de vezes mais rápido do que ocorreriam sem a sua intervenção. As enzimas são, por isso, essenciais à vida, uma vez que o teu organismo não pode esperar dias, semanas, ou anos para receber os importantes produtos das reações bioquímicas.
Minúsculos Auxiliares
Muitos outros cientistas estão a descobrir maneiras de poder utilizar a mão-de-obra bacteriana. Alguns químicos estão a usar enzimas de bactérias para degradar agentes biologicamente nocivos. O mortífero gás Sarin libertado pela seita Aum Shinrikyo em 1995 no sistema de metro de Tóquio, é um exemplo. Incluído numa classe de moléculas designadas por organofosfatos, o gás Sarin atua nos circuitos nervosos vitais dos organismos de humanos e animais; a exposição a quantidades muito reduzidas pode matar uma vítima em tão pouco tempo como 5 minutos.
Contudo, felizmente certos tipos de bactérias produzem uma enzima designada por fosfotriesterase (PTE), que inativa o gás Sarin e outras moléculas de organofosfatos semelhantes, algumas das quais estão presentes em inseticidas, mas são centenas de vezes menos tóxicas para humanos. Certos organofosfatos, como o inseticida malationa, matam insetos porque estes não possuem uma enzima que degrada este químico. Desde há muitos anos que Frank Raushel da Texas A&M University, College Station se dedica ao estudo da enzima PTE. Recentemente, ele e a sua colega Hazel Holden da University of Wisconsin-Madison superaram um importante obstáculo: identificaram a estrutura tridimensional — uma "foto molecular" — desta enzima. Esta informação ajudará os cientistas a compreender como funciona a enzima — e pode revelar como criar uma que funcione ainda melhor.
Os Metais Podem Fazer-te Bem...
Enzimas como a PTE dependem de um tipo especial de assistência molecular para desempenhar as suas funções de um modo eficiente. Metais, como o ferro, o zinco e o cobre desempenham papéis fundamentais em algumas das reações enzimáticas que mantêm o metabolismo do organismo. O ferro, por exemplo, ajuda a proteína hemoglobina a transportar oxigénio para os órgãos. Muitos metais atuam estabilizando as formas das enzimas. Mas a reação do organismo aos metais — alguns dos quais podem ser altamente tóxicos quando em excesso — é um assunto complicado. Em alguns casos, as células exercem um controlo particularmente firme, garantido que apenas um ou dois átomos do metal estejam presentes no interior de uma célula.
O cobre é um desses casos. Caranguejo e lagosta, mais do que um petisco de Verão, são também uma boa fonte dietária deste metal. Sim, os constituintes das moedas são cruciais à vida — o cobre é um importante auxiliar de muitas enzimas celulares, incluindo uma denominada superóxido dismutase (SOD), que elimina perigosos “radicais livres”, que se acumulam no interior das células. Problemas com a SOD foram associados a algumas formas hereditárias de esclerose lateral amiotrófica (ELA), também designada por doença de Lou Gehrig. Apesar de o cobre ser indispensável à vida, é uma substância potencialmente tóxica que — quando no local errado da célula — pode danificar outras moléculas e, em alguns casos, causar mesmo doença. Uma equipa de cientistas, incluindo Valeria Culotta da Johns Hopkins Bloomberg School of Public Health, Baltimore e Thomas O'Halloran e Amy Rosenzweig da Northwestern University, Evanston, Illinois, decifraram a estrutura tridimensional de uma proteína de levedura que atua como "chaperone molecular" do cobre. Esta proteína transporta o cobre até à enzima SOD e protege o metal de interações celulares indesejáveis ao longo do percurso. Na ELA, os investigadores suspeitam que SOD alterada — quando associada ao cobre de que necessita para ficar ativa — fica fora de controlo e provoca danos celulares. Conhecer mais sobre o funcionamento do conjunto SOD-chaperone do cobre, irá permitir aos designers de medicamentos vislumbrar uma forma de interferir com esta interação molecular em pacientes com a doença de Lou Gehrig.
Uma Língua Eletrónica

Marsha Miller
Embora bastante afastada da verdadeira, uma nova língua artificial promete fazer muito mais do que saborear hambúrgueres e lamber selos. O químico Eric Anslyn da Texas University at Austin e os seus colegas desenvolveram um protótipo de "língua", que é um biossensor aplicado à análise de líquidos; uma pequenina placa de silício com esferas de deteção embutidas que adquirem coloração na presença de químicos específicos. A língua eletrónica original de Anslyn era apenas capaz de diferenciar entre ácidos, açúcares simples e determinadas moléculas carregadas eletricamente. Contudo, em teoria, podem ser adicionados ao chip muitos mais micro-detetores químicos, permitindo ao aparelho distinguir diversos componentes de uma solução. De facto, uma língua eletrónica pode ser algo realmente útil, se se considerar que pode ser utilizada para "provar" soluções como sangue, urina e água poluída, por exemplo. Claro que o sistema também pode ser usado para assegurar controlo de qualidade em substancias muito mais palatáveis, como refrigerantes.
...ou Os Metais Podem Fazer-te Mal
Apesar de ser evidente que o organismo não funcionaria adequadamente sem uma determinada quantidade de um conjunto específico de metais, alguns podem ser efetivamente tóxicos para o organismo. Mesmo os metais que são necessários podem trazer problemas quando estão em quantidades excessivas. Uma vez que os metais são elementos (as unidades estruturais de todos os compostos químicos), como compostos básicos terrestres, não podem ser degradados (como são, por exemplo, as proteínas e gorduras). Por isso, o nosso organismo é muito cuidadoso na condução destes materiais potencialmente tóxicos até aos seus destinos no interior das células. Tal como acontece com o cobre, muitos outros metais são "acompanhados" por moléculas protetoras tipo chaperone.
Alguns metais tóxicos, pelo contrário, não são bons independentemente da sua quantidade. Podem afetar enzimas importantes, comprometendo as suas funções. Por exemplo, chumbo de origem ambiental pode interferir com a síntese de um componente vital da hemoglobina, designado por grupo heme, impedindo o transporte de oxigénio pelo sangue. Alguns metais podem ficar contidos no interior de compartimentos celulares denominados organelos e impossibilitar o normal funcionamento celular. Algumas formas de mercúrio podem ser mortíferas, provocando danos irreversíveis no cérebro. Os cientistas acreditam que alguns metais altamente tóxicos, tal como o arsénico, podem também causar cancro a nível da pele e dos pulmões.
METAIS NA SAÚDE E NA DOENÇA
| METAL (Símbolo Químico) | Onde está? | O que faz? | Como é que o obtenho? |
|---|---|---|---|
| Metais "Saudáveis" | |||
| Ferro (Fe) | Liga-se a enzimas por todo o organismo (ex: hemoglobina, óxido nítrico sintase) | Auxilia no transporte de oxigénio e de certos mensageiros químicos | Carnes (mais elevado em carne de vaca e de porco e em fígado), feijão, melaço, espinafre |
| Cobre (Cu) | Liga-se a enzimas por todo o organismo (ex: superóxido dismutase) | Protege o organismo de danos provocados por radicais livres | Marisco (caranguejo, lagosta), feijão seco, noz |
| Zinco (Zn) | Liga-se a enzimas por todo o organismo, ao DNA e a algumas hormonas (ex: insulina) | Intervém na maturação sexual e na regulação hormonal; ajuda algumas proteínas a ligar-se ao DNA | Marisco (ostras), grão-de-bico, feijão cozido, cereais integrais, nozes |
| Sódio (Na) Potássio (K) |
Por todo o organismo (Na no exterior das células, K no interior das células) | Auxilia na transmissão de sinais elétricos ao longo dos nervos e no coração | Na: sal de cozinha e bicarbonato de sódio K: banana, laranja, abacate |
| Cálcio (Ca) | Ossos, músculos | Intervém em funções musculares e nervosas e na coagulação | Laticínios, brócolos, figos |
| Cobalto (Co) | É o componente central da vitamina B12 | Indispensável à formação de glóbulos vermelhos | Carnes, laticínios, hortaliças |
| Metais "Não Saudáveis" | |||
| Arsénico (Ar) | Rochas, solo | Pode ser cancerígeno e provocar a morte | Tóxico |
| Chumbo (Pb) | Tintas antigas (antes de 1973) | Pode provocar cancro, danos neurológicos e morte | Tóxico |
| Mercúrio (Hg) | Peixe contaminado | Liga-se a moléculas com enxofre nos organelos; pode provocar danos neurológicos e morte | Tóxico |
Caixa de Questões: Fábricas do Futuro
A Química da Saúde perguntou a Mary Lidstrom, Professora de Engenharia Química e Microbiologia na University of Washington, Seattle, "Quais são as novidades para si no horizonte da biotecnologia?". A biorremediação não é necessariamente o interesse mais imediato, diz Lidstrom, explicando que os engenheiros nas empresas estão prestes a conseguir que determinadas bactérias — especialmente do tipo das que ela estuda — limpem o ambiente. Para ela, o verdadeiro interesse reside em conseguir que as bactérias produzam novos materiais de uma forma mais económica e eficiente, utilizando matérias-primas não tóxicas e não produzindo resíduos tóxicos. No seu próprio laboratório, Lindstrom passa grande parte do seu tempo a tentar convencer as bactérias a fazerem coisas que não era suposto fazerem.
E as bactérias — elas têm um metabolismo tão espantoso. São capazes de quase tudo.

QS: O que é que o futuro reserva para o tipo de biotecnologia em que está a trabalhar?
Lidstrom: O maior desafio consiste no afastamento da indústria química da petroquímica. O nosso objetivo é transformar bactérias em fábricas químicas.
QS: Em que é que isso iria ajudar?
Lidstrom: Poder-se-ia utilizar açúcares simples, como a glicose, ou outros recursos potencialmente renováveis — como o metanol — como matérias-primas.
QS: Quais são os desafios que se colocam aos cientista a trabalhar nesta área?
Lidstrom: O problema é que, presentemente, isto não é economicamente viável — o desafio consiste em como alterar estas bactérias. A natureza não as fez para fazerem isto.
QS: O que é que a atraiu para a ciência?
Lidstrom: Eu cresci numa quinta de produção de gado em Oregon, onde estava sempre próxima da biologia. Sempre fiquei fascinada com o modo como as coisas funcionam e o porquê — como é que a luz que incide numa folha a faz abrir-se? E tive excelentes professores de ciências a alimentar os meus interesses.
QS: Porquê microbiologia?
Lidstrom: Não há sangue! E as bactérias — elas têm um metabolismo tão espantoso. São capazes de quase tudo.
Compreendeste?
Quais são os substratos utilizados pela enzima metano monooxigenase? Quais são os produtos criados por esta enzima?
Quais são as vantagens da química combinatória relativamente aos métodos mais tradicionais na pesquisa de novos medicamentos?
Refere um antibiótico produzido por bactérias do solo.
Descreve dois processos em que o teu organismo utiliza metais para funcionar adequadamente.
Comenta as vantagens da utilização de organismos vivos para a produção de medicamentos ou outros produtos de consumo.


