A Nova Genética
Capítulo 1: Como funcionam os genes
Há muitos anos que sabemos que os seres vivos herdam características dos seus progenitores. Essa observação empírica levou à agricultura, isto é, à cuidadosa reprodução de animais e plantas com as características desejáveis. No entanto, levou algum tempo até se chegar aos detalhes deste processo. Até meados do século XX, os cientistas não percebiam exatamente como é que as características eram passadas à geração seguinte.

Agora está claro que são os genes que transportam as nossas características de geração em geração e que os genes são feitos de ácido desoxirribonucleico (DNA). Mas, os genes propriamente ditos, não trabalham. Na verdade, eles servem de livro de instruções para a construção de moléculas funcionais, tais como o ácido ribonucleico (RNA) e as proteínas, que participam nas reacções químicas no nosso corpo.
As proteínas também desempenham muitas outras tarefas. São os principais constituintes do corpo, formando a arquitetura e componentes estruturais da célula. Mas, há algo que as proteínas não conseguem fazer: cópias de si próprias. Quando uma célula precisa de mais proteínas, usa as instrução de fabrico codificadas no DNA.
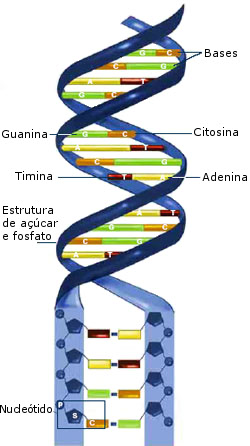
O código de DNA de um gene, isto é, a sequência dos seus constituintes básicos, adenina (A), timina (T), citosina (C) e guanina (G) (coletivamente chamados nucleótidos), soletra a ordem exata dos constituintes básicos das proteínas, os aminoácidos.
Ocasionalmente, há algum "erro tipográfico" na sequência de DNA de um gene. A este erro (que pode ser uma alteração, uma falha ou uma duplicação) chama-se mutação.
A existência de uma mutação pode fazer com que um gene codifique uma proteína defeituosa ou que não funcione. Por vezes, o erro leva a que nenhuma proteína seja pro-duzida.
Mas nem todas as alterações no DNA são prejudiciais. Algumas mutações não têm qualquer efeito e outras levam à produção de novas versões de proteínas que conferem uma vantagem na sobrevivência dos organismos que as possuem. Ao longo do tempo, as mutações são o material a partir do qual novas formas de vida evoluem (veja o Capítulo 3, "A árvore genética da vida").
Genética no jardim

Em 1900, três cientistas europeus descobriram, de modo independente, um artigo científico publicado 35 anos antes. Escrito por Gregor Mendel, um monge austríaco que também era cientista, o artigo descrevia uma série de experiências feitas com ervilheiras que cresciam nos jardins da abadia.
Mendel tinha estudado a hereditariedade de duas características fáceis de observar nas ervilheiras: a cor da flor (branca ou roxa) e a textura das ervilhas (lisa ou rugosa). Mendel estudou muitas gerações de ervilheiras e percebeu que estas características eram passadas à geração seguinte de forma ordenada e em proporções previsíveis.

Quando cruzava ervilheiras de flor roxa com ervilheiras de flor branca, a geração seguinte só apresentava flores roxas. Mas as instruções para produzir flores brancas continuavam escondidas algures nas ervilhas dessa geração porque, quando essas ervilheiras de flor roxa se cruzavam, alguns dos seus descendentes tinham flores brancas. Para além disso, as plantas da segunda geração exibiam as cores num padrão previsível. Em média, 75% das plantas da segunda geração tinham flores roxas e 25% tinham flores brancas. Essas taxas eram persistentes e reproduziam-se em todas as repetições da experiência.
Ao tentar solucionar o mistério das cores ausentes, Mendel imaginou que as células reprodutoras da ervilheira poderiam conter "fatores" discretos, cada um dos quais seria, específico para uma característica particular, como a das flores brancas. Mendel argumentava que estes fatores, o que quer que fossem, deveriam ser matéria física, porque passavam de pais para filhos com uma ordem matemática. Só muitos anos depois, quando se descobriu este trabalho, é que esses fatores foram chamados genes.
Os primeiros geneticistas rapidamente descobriram que as regras matemáticas da hereditariedade de Medel não se aplicavam só às ervilhas, mas também a todas as plantas, animais e pessoas. A descoberta de uma regra quantitativa para a hereditariedade foi decisiva. Revelou que havia um princípio geral comum que governava o crescimento e desenvolvimento de toda a vida na Terra.
Belo DNA
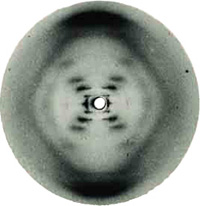
Até à década de 1950, os cientistas sabiam bastante sobre a hereditariedade, mas não faziam ideia de qual o aspeto do DNA. Para aprender mais sobre o DNA e a sua estrutura, alguns cientistas experimentaram usar raios-X como um método de fotografia molecular.

ARQUIVOS DO COLD SPRING HARBOR LABORATORY
Rosalind Franklin, uma química física que trabalhava com Maurice Wilkins no King's College, em Londres, esteve entre os primeiros cientistas a usar este método para analisar material genético. As suas experiências originaram aquelas que foram consideradas na época "as mais belas fotos em raios-X alguma vez feitas de uma substância."
Outros cientistas, incluindo o zoólogo James Watson e o físico Francis Crick, ambos a trabalhar na University of Cambridge, no Reino Unido, estavam também a tentar determinar a forma do DNA. Em resultado disso, esta investigação revelou uma das descobertas científicas mais profundas do século XX: que o DNA é uma dupla hélice.
Por este trabalho, o Prémio Nobel em Fisiologia e Medicina de 1926 foi atribuído a Watson, Crick e Wilkins. Embora Franklin não tenha ganho uma parte do prémio, devido à sua morte aos 38 anos, ela é amplamente reconhecida como tendo tido um papel significativo na descoberta.
COLEÇÕES ESPECIAIS DAS BIBLIOTECAS DA OREGON STATE UNIVERSITY
A dupla hélice em forma de escadaria espiralada alcançou o estuto global como símbolo do DNA. Mas o que é realmente belo na descoberta desta estrutura em escada retorcida não é só o seu aspeto. A estrutura do DNA deu aos investigadores uma lição fundamental em genética: mostrou-lhes que as duas cadeias ligadas eram complementares e, deste modo, foi desvendado o segredo de como a informação genética é armazenada, transferida e copiada.
Em genética, a complementaridade implica que, quando se conhece a sequência de nucleótidos de uma cadeia, conhece-se a sequência de nucleótidos da outra cadeia: A alinha-se sempre com T e C liga-se sempre a G (veja o desenho).
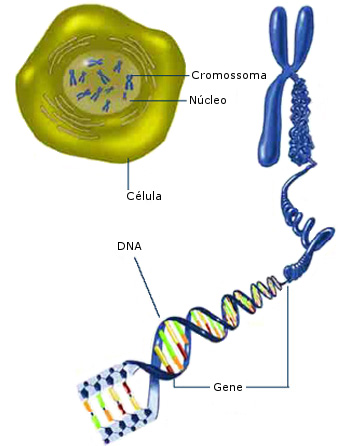
As longas cadeias de nucleótidos formam genes e os grupos de genes são "empacotados" em estruturas chamadas cromossomas. Todas as células do nosso corpo, com exceção dos gâmetas e glóbulos vermelhos, contêm um conjunto completo de cromossomas no núcleo.
Se os cromossomas de uma das nossas células fosse desenrolado e esticado, o DNA teria cerca de dois metros de comprimento. Se todo o DNA do nosso corpo fosse alinhado desta forma, mediria cerca de 108 mil milhões de quilómetros! Isso corresponde a quase 150 000 viagens de ida e volta à Lua.
Estrutura do DNA
Imitador
LABORATÓRIO DE CITOGENÉTICA, BRIGHAM AND WOMEN'S HOSPITAL
É espantoso pensar que o nosso corpo é constituído por biliões de células. Mas, o que é ainda mais incrível, é que tudo começa com uma só célula. Como é que ocorre esta expansão tão ampla?
À medida que um embrião se desenvolve, as suas células reproduzem-se. Mas, antes de uma célula se dividir em duas células quase idênticas, primeiro tem que fazer uma cópia do seu DNA, para que haja um conjunto completo de genes que passe para cada uma das novas células.
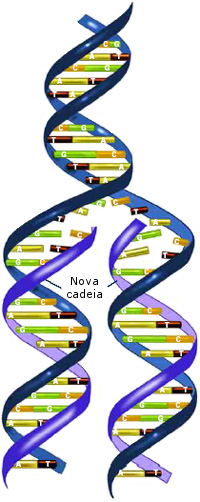
Para fazer uma cópia de si mesma, a retorcida e compactada dupla hélice de DNA tem que se desenrolar e separar as suas duas cadeias. Cada cadeia passa a servir de molde para uma nova cadeia, de forma que as duas novas moléculas de DNA têm uma cadeia nova e uma cadeia antiga.
A cópia é fruto da atividade de uma máquina proteica celular chamada DNA polimerase, que lê a cadeia molde de DNA e a ela une a nova cadeia complementar. O processo, chamado replicação, é extraordinariamente rápido e preciso, embora ocorram erros ocasionais, como deleções ou duplicações. Felizmente, há um corretor celular que deteta e corrige quase todos este erros.
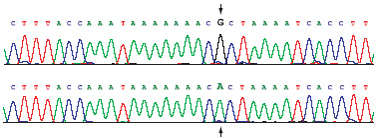
Os erros que não são corrigidos podem levar a doenças como cancro e certas doenças genéticas. Por exemplo, a anemia de Fanconi, o envelhecimento precoce e ou-tras doenças em que as pessoas são extrema-mente sensíveis à luz ou a alguns produtos químicos.
A cópia do DNA não é a única fase em que este sofre danos. A exposição prolongada ao Sol sem proteção também pode causar alterações no DNA que levam a cancro de pele e as toxinas do fumo do cigarro podem provocar cancro do pulmão.
Pode então parecer irónico que muitos medicamentos usados no tratamento do cancro atuem atacando o DNA. Isso ocorre porque os medicamentos usados em quimioterapia interferem com o processo de cópia do DNA, que é muito mais rápido nas células cancerígenas em divisão do que nas outras células do corpo. O problema é que a maioria destes medicamentos também afetam as células normais que crescem e se dividem frequentemente, como as células do sistema imunitário e as do cabelo.
Uma melhor compreensão da replicação do DNA pode ser a chave para conseguir limitar a ação dos medicamentos somente às células cancerígenas.
Digamos que é igual
Depois de copiado o DNA, o desafio seguinte para a célula é assegurar que as duas células-filhas recebam a quantidade adequada de material genético.
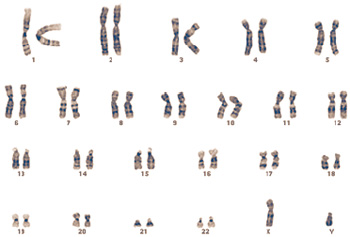
A maioria das nossas células são diploides ("di" significa dois e "ploide" refere-se aos conjuntos de cromossomas) porque têm dois conjuntos de cromossomas (23 pares). Os óvulos e os espermatozoides são diferentes; são conhecidas como células haploides. Cada célula haploide tem apenas um conjunto de 23 cromossomas, de forma a que na fertilização as contas batam certo: um óvulo haploide combina-se com um espermatozoide haploide e forma uma célula diploide com o número correto de cromossomas: 46.
Os cromossomas são numerados de 1 a 22, de acordo com o seu tamanho, sendo o 1 o maior. O 23º par, conhecidos como cromossomas sexuais, são chamados X e Y. Nos seres humanos, as anomalias no número de cromossomas ocorrem geralmente durante a meiose, quando a célula reduz o número de cromossomas, de diploide a haploide, para gerar óvulos ou espermatozoides.
O que é que acontece quando um óvulo ou espermatozoide tem um número erróneo de cromossomas? É frequente isto acontecer?

A bióloga molecular Angelika Amon, do Massachusetts Institute of Technology, em Cambridge, diz que os erros de divisão do DNA entre células-filhas durante a meiose são a principal causa das malformações e abortos naturais. As estimativas atuais dizem que 10% dos embriões têm um número incorreto de cromossomas. A maioria não chega a nascer.
Nas mulheres, a probabilidade de erros na divisão dos cromossomas aumenta com a idade. Um em cada 18 bebés nascidos de mães com mais de 45 anos tem três cópias do cromossoma 13, 18 ou 21, e este desequilíbrio pode causar problemas. Por exemplo, três cópias do cromossoma 21 leva ao Síndrome de Down.
Para facilitar o seu trabalho, Amon – como muitos outros cientistas – estuda células de levedura, que separam os seus cromossomas quase como as células humanas, com a diferença de o fazerem muito mais rapidamente. Uma célula de levedura copia o seu DNA e gera células-filhas em cerca de 90 minutos, enquanto que nas células humanas o processo demora um dia.
As leveduras que ela usa são do mesmo tipo das que os padeiros usam para fazer pão e os cervejeiros para fazer cerveja!
Amon fez avanços significativos na compreensão dos detalhes da meiose. A sua investigação mostra como, em células saudáveis, complexos proteicos que atuam como cola, chamados coesinas, libertam os pares de cromossomas no momento certo. Isto permite que os cromossomas se separem corretamente.
Estas descobertas têm importantes implicações para a compreensão e tratamento da infertilidade, malformações e cancro.
Meiose
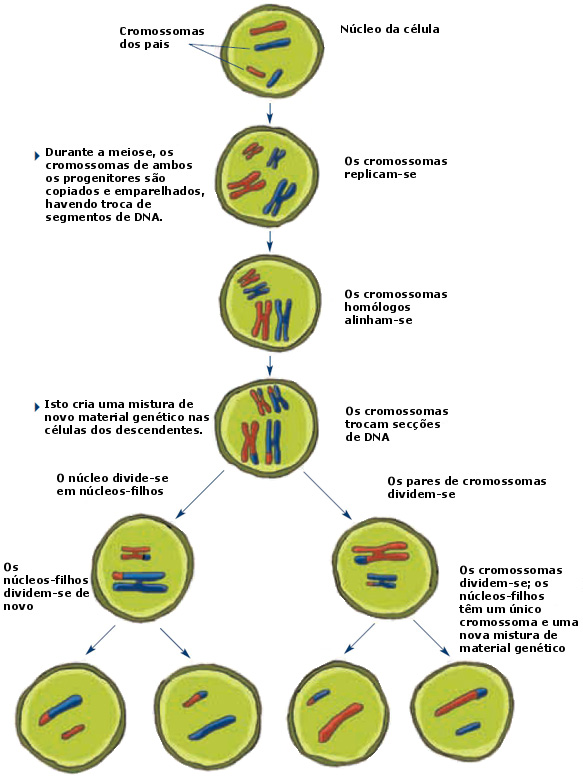
Receber a mensagem
Já descrevemos o DNA, as suas propriedades básicas e o modo como os nossos corpos o produzem. Mas, como é que o DNA funciona como linguagem da vida? Como é que obtemos uma proteína a partir de um gene?
Há dois grandes passos no fabrico de uma proteína. O primeiro é a transcrição, onde a informação codificada no DNA é copiada para o RNA. Os nucleótidos de RNA são complementares aos do DNA: um C na cadeia de RNA corresponde a um G na cadeia de DNA.
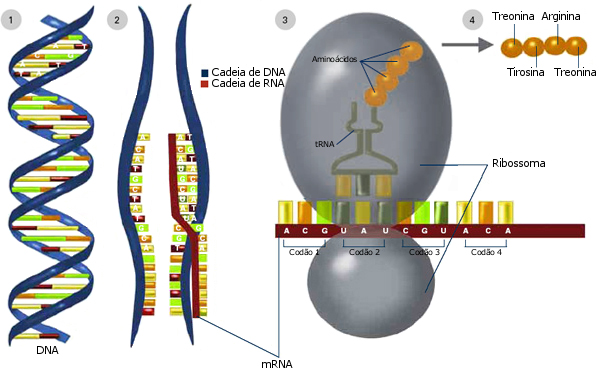
A única diferença é que, no RNA, em vez de um T, ao A do DNA liga-se um nucleótido chamado uracilo (U).
A máquina proteica chamada RNA polimerase lê o DNA e faz uma cópia de RNA. Esta cópia é chamada de RNA mensageiro, ou mRNA, porque entrega a mensagem do gene à maquinaria que fabrica as proteínas.
Neste momento deve estar a questionar-se porque é que todas as células do corpo humano não são exatamente iguais, já que todas têm o mesmo DNA. O que é que faz com que uma célula do fígado seja diferente de uma do cérebro? Como é que as células do coração fazem contrair este órgão, enquanto que as da pele nos fazem suar?
As células podem ter aspeto e comportamento diferentes, e desempenhar funções completamente distintas, porque cada célula "liga", ou expressa, apenas aqueles genes que necessita para a sua função.
STEVEN BLOCK
E isto acontece porque a RNA polimerase não atua sozinha, mas sim em conjunto com muitas proteínas auxiliares. Embora a parte central da RNA polimerase seja a mesma em todas as células, as auxiliares variam nos diferentes tipos de células do corpo.
Sendo este um processo essencial à vida, seria de pensar que os cientistas já soubessem muito sobre o funcionamento da transcrição. Embora tenhamos os conhecimentos básicos – os biólogos já estudam a transcrição genética pela RNA polimerase desde que as proteínas foram descobertas em 1960 – alguns detalhes são ainda obscuros.
O maior obstáculo ao conhecimento tem sido a falta de ferramentas. Até há pouco tempo, os cientistas não tinham conseguido uma imagem a nível atómico dos aglomerados proteicos gigantes de RNA polimerase dentro das células, para poderem perceber como é que as muitas peças desta incrível máquina viva cumprem a sua função tão bem.
Mas, graças a avanços tecnológicos espetaculares, a nossa compreensão está a melhorar rapidamente. Já dispomos de novas fotos de raios-X que são bem mais sofisticadas que aquelas que revelaram a estrutura do DNA. Roger Kornberg, da Stanford University, na Califórnia, usou esse tipo de métodos para determinar a estrutura da RNA polimerase. Este trabalho valeu-lhe o Prémio Nobel da Química em 2006. Para além disso, poderosos microscópios e outras ferramentas que nos permitem ver uma molécula de cada vez, dão-nos uma nova perspetiva da RNA polimerase em funcionamento, a ler o DNA e a produzir RNA.
Por exemplo, Steven Block, também de Stanford, tem usado uma técnica da Física chamada armadilha ótica para seguir a RNA polimerase à medida que esta avança ao longo do DNA. Block e a sua equipa lograram desenhar um microscópio especializado e de tal modo sensível, que permite observar, em tempo real, o movimento de uma única polimerase a deslizar ao longo de um gene de um cromossoma.
Os cientistas descobriram que as moléculas de RNA polimerase se comportam como "aranhas a pilhas" à medida que "rastejam" pela escada de DNA, adicionando um nucleótido de cada vez à cadeia de RNA. Block suspeita que a enzima funciona quase como um motor, sendo alimentada pela energia libertada durante a síntese química do RNA.
O trabalho de corta-e-cose da Natureza
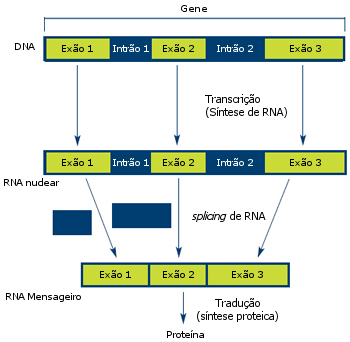
Há vários tipos de RNA que têm papéis chave na produção de uma proteína. O gene transcrito (o mRNA) transfere informação do DNA no núcleo para os ribossomas, que fazem as proteínas. O RNA ribossómico constitui cerca de 60% dos ribossomas. E o RNA de transferência transporta os aminoácidos para os ribossomas. Como se pode ver, os três tipos celulares de RNA aliam-se para a produção de novas proteínas.
Mas a viagem do gene à proteína não é assim tão simples como fizemos parecer até agora. Após a transcrição, o mRNA sofre vários processos até chegar à fase de produção de uma proteína. Por exemplo, o material genético dos seres humanos e outros eucariotas (organismos com núcleo) inclui muito DNA que não codifica proteínas. Parte deste DNA está mesmo no meio de genes.
Para distinguir os dois tipos de DNA, os cientistas chamam às sequências codificantes do genes exões, e aos segmentos que estão no meio intrões (sequências intermédias).
Se a RNA polimerase transcrevesse um gene com intrões do princípio ao fim, o RNA seria complementar aos intrões e aos exões.
Para que o mRNA dê origem a uma proteína funcional, a célula deve cortar as secções intrónicas e depois unir só os exões (veja o esquema). A este processo chama-se splicing do RNA.
O splicing tem que ser extremamente rigoroso. Um erro neste processo, mesmo que resulte apenas na deleção de um nucleótido num exão ou na adição de um nucleótido num intrão, desalinhará toda a sequência. O resultado é geralmente uma proteína anormal ou nenhuma proteína. Por exemplo, há uma variante da doença de Alzheimer que é causada por este tipo de erro de splicing.
A bióloga molecular Christine Guthrie, da University of California, em San Francisco, quer perceber melhor o mecanismo de remoção de intrões do RNA e descobrir como é que este se mantém tão rigoroso.
Para isso, usa leveduras nas suas experiências. Tal como o DNA humano, o DNA das leveduras tem intrões, mas estes estão em menor número e têm uma estrutura mais simples, pelo que são mais fáceis de estudar. Guthrie pode identificar quais os genes necessários ao splicing procurando leveduras anormais que deturpam o splicing.
Mas então, porque é que existem intrões se eles só servem para serem cortados? Sem os intrões as células não necessitariam do processo de splicing, nem da sua contínua monitorização.
Na verdade, o splicing também permite às células a criação de mais proteínas.
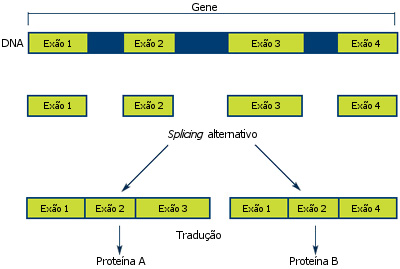
Pense em todos os exões de um gene. Se uma célula unir os exões 1, 2 e 4, excluindo o exão 3, o mRNA vai levar ao fabrico de uma determinada proteína. Mas, se em vez disso, se a célula unir os exões 1, 2 e 3, desta vez excluindo o exão 4, então o mRNA será traduzido numa proteína diferente (veja o esquema).
Ao cortar e unir os exões em diferentes posições, o que os cientistas chamam splicing alternativo, a célula pode criar proteínas diferentes a partir do mesmo gene. O splicing alternativo é um dos motivos pelos quais as células humanas, que têm cerca de 20 000 genes, podem fabricar centenas de milhares de proteínas diferentes.
Agora, todos juntos
Até há pouco tempo, os investigadores estudavam os genes, e as proteínas por eles codificadas, um de cada vez. Agora, podem ver como um grande número de genes e proteínas atuam e interagem. Isto dá-lhes uma melhor imagem do que se passa no ser vivo.
Já é possível identificar todos os genes que são transcritos numa célula ou num órgão, como o coração. E, embora os cientistas não possam dizer, num dado momento, o que é que se está a passar em cada célula do nosso corpo enquanto lemos este texto ou caminhamos na rua, podem fazer uma espécie de "scan corporal" em organismos unicelulares mais simples, como as leveduras.
Ao usar a técnica de análise de localização genómica (genomewide location analysis), Richard Young, do Massachusetts Institute of Technology, descobriu um "código regulador" das células de leveduras, que têm mais de 6000 genes no seu genoma. A técnica de Young permitiu-lhe determinar os locais exatos onde as proteínas auxiliares da RNA polimerase se posicionam no DNA e dizem à RNA polímerase para iniciar a transcrição de um gene.
Como Young realizou a experiência com leveduras expostas a diferentes condições, foi capaz de descobrir as diferenças entre padrões de transcrição de uma célula que está sob stress (por exemplo, num ambiente seco) ou a crescer numa solução rica em açúcar e nutrientes. Se este tipo de análise fosse feita para um gene de cada vez, com a tecnologia de ponta de há alguns anos, demoraria centenas de anos.
Após demonstrar que esta técnica funciona em leveduras, Young deu mais um passo na sua investigação e usou uma variação do método para analisar todo o genoma humano em pequenas amostras de células retiradas do pâncreas e do fígado de pessoas com diabetes tipo 2. Usou os resultados para identificar os genes que não são transcritos corretamente nestes doentes.
Esta informação dá-nos uma importante ferramenta para perceber como é que a diabetes e outras doenças são influenciadas por genes defeituosos. Construindo modelos de como os genes respondem em diferentes situações, os investigadores podem aprender a parar ou fazer funcionar certos genes, alterando o rumo de uma doença, ou até mesmo preveni-la.
Nós e a genética: Genética de berçário

Embora a maior parte da investigação genética seja feita com organismos de laboratório, tubos de ensaio e placas de Petri, os seus resultados têm consequências reais para as pessoas. O nosso primeiro encontro com uma análise genética aconteceu provavelmente logo após o nascimento, quando um médico ou uma enfermeira recolheu uma gota de sangue do calcanhar do nosso pezinho.
As análises realizadas com aquela única gota de sangue podem diagnosticar certas doenças genéticas raras, bem como problemas metabólicos, como a fenilcetonúria (PKU).
Este tipo de análise aos recém-nascidos iniciou-se na década de 1960, em Massachusetts, com o teste para a PKU, uma doença que afeta 1 em cada 14 000 pessoas. A PKU é causada por uma enzima que não funciona corretamente devido a uma mutação genética. Aqueles que nascem com este problema não conseguem metabolizar o aminoácido fenilalanina, que está presente em muitos alimentos. Se não for tratada, a PKU pode levar a atrasos mentais e danos neurológicos. Mas, se se seguir uma dieta especial, podem-se prevenir estas consequências. Este teste fez uma grande diferença para muitas vidas.
A testagem dos recém-nascidos é gerida por cada Estado (nos Estados Unidos da América). Isto significa que cada Estado determina quais as doenças a testar no bebé. Atualmente, nos Estados Unidos da América (EUA), são testadas entre 28 e 54 doenças. Em todos os Estados, está contemplada a PKU.
Embora algumas pessoas defendam o alargamento da testagem de doenças genéticas em recém-nascidos, outras questionam o valor dos testes a doenças para as quais ainda não há tratamento. Um outro problema é o tratamento desnecessário de algumas crianças que têm versões "leves" de algumas doenças genéticas.
Em 2006, o Comité de Aconselhamento sobre Doenças Genéticas em Recém-nascidos e Crianças, que assiste o Ministério da Saúde dos EUA, recomendou um padrão nacional de testagem para 29 doenças, que incluiria alguns problemas comuns de surdez e doenças metabólicas muito raras.
Achado na tradução
A ESTRUTURA DO RIBOSSOMA FOI CEDIDA POR JAMIE CATE, MARAT YUSUPOV, GULNARA YUSUPOVA, THOMAS EARNEST E HARRY NOLLER. O TRABALHO GRÁFICO É CORTESIA DE ALBION BAUCOM, DA UNIVERSITY OF CALIFORNIA, EM SANTA CRUZ.
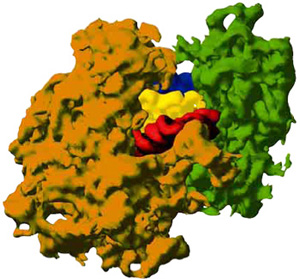
Depois da leitura do gene pela RNA polimerase e do splicing do RNA, o que é que acontece, a seguir, na viagem que vai do gene à proteína? O passo seguinte é a leitura da informação contida no RNA e o encaixe dos "blocos de construção" de uma proteína. Este processo chama-se tradução e os seus atores principais são o ribossoma e os aminoácidos.
Os ribossomas são das maiores e mais intrincadas estruturas da célula. Os ribossomas das bactérias não só contêm quantidades enormes de RNA, como também mais de 50 proteínas diferentes. Os ribossomas humanos têm ainda mais RNA e entre 70 a 80 proteínas diferentes!
Harry Noller, da University of California, em Santa Cruz, descobriu que o ribossoma tem vários papéis chave quando traduz o código genético do mRNA. À medida que o mRNA passa pela máquina ribossómica de fazer proteínas, o ribossoma lê a sequência do mRNA e ajuda a reconhecer e recrutar o tRNA que transporta o aminoácido correto para aquele código. O ribossoma também une cada aminoácido adicional, fazendo crescer a cadeia proteica (veja o desenho).
Durante muitos anos, os cientistas pensavam que, embora o RNA fizesse parte do ribossoma, a parte proteica do ribossoma era a que tinha mais funções. No entanto, Noller propôs que talvez fosse o RNA, e não as proteínas, a desempenhar a função do ribossoma. No início, a sua ideia não era popular porque, naquela época, pensava-se que o RNA não poderia desempenhar funções complexas.

Contudo, algum tempo depois, o consenso mudou. Sidney Altman, da Yale University, em New Haven, Connecticut, e Thomas Cech, que estava na University of Colorado, em Boulder, descobriram que o RNA pode desempenhar funções tão complexas como as das enzimas proteicas. A sua descoberta do "RNA como enzima" foi uma reviravolta no mundo da investigação e valeu-lhes o Prémio Nobel da Química em 1989.
Noller e outros investigadores continuaram a estudar os difíceis ribossomas. Em 1999, demonstrou como as diferentes partes do ribossoma bacteriano interagem entre si e como o ribossoma interage com moléculas envolvidas na síntese proteica. Estes estudos foram a prova quase definitiva de que o mecanismo fundamental da tradução era realizado pelo RNA e não pelas proteínas do ribossoma.
Surpresas do RNA
Mas qual é o RNA ribossómico que está a fazer este trabalho? A maioria dos cientistas assumiu que os nucleótidos de RNA localizados no interior do complexo ribossómico (aqueles que têm a mesma sequência em todas as espécies, das bactérias até às pessoas) seriam os mais importantes na construção da proteína.
No entanto, uma investigação recente de Rachel Green, que trabalhou com Noller antes de ir para a Johns Hopkins University, em Baltimore, Maryland, não mostrou isso. Green descobriu que esses nucleótidos de RNA não são necessários para a construção da proteína. Em vez disso, ela descobriu que esses nucleótidos têm uma função completamente diferente: ajudam a proteína em formação a sair do ribossoma.
Noller, Green e centenas de outros cientistas trabalham com ribossomas de bactérias. E porque é que nos deveríamos de preocupar com o modo como as bactérias criam proteínas a partir de genes?
Uma das razões é que este conhecimento é importante para sabermos como interromper as acções de microorganismos causadores de doenças. Por exemplo, antibióticos como a eritromicina e a neomicina funcionam atacando os ribossomas das bactérias, que são suficientemente diferentes dos nossos ribossomas para que as nossas células não sejam afetadas por estes medicamentos.
À medida que os investigadores adquirem mais informação sobre a tradução bacteriana, este conhecimento pode levar à descoberta de mais antibióticos para as pessoas.
São precisos novos antibióticos com urgência porque muitas bactérias desenvolveram resistência àqueles de que dispomos. Esta resistência é por vezes resultado de alterações no RNA ribossómico da bactéria. Pode ser difícil encontrar as pequenas, mas cruciais, alterações que levam à resistência. Portanto, é importante encontrar novas formas de bloquear a tradução bacteriana.
Green está também a trabalhar nesse problema. A estratégia dela é provocar mutações aleatórias nos genes da bactéria que afetem os seus ribossomas. E se a mutação altera o ribossoma de tal forma que este já não produz proteínas? Então a bactéria não cresce e Green não a encontra.
Mas, usando alguns truques moleculares, Green encontrou uma forma de salvar algumas bactérias com ribossomas defeituosos, de modo a que estas pudessem crescer. Enquanto que algumas das bactérias têm alterações no RNA ribossomal que as tornam resistentes a certos antibióticos (logo, não são bons alvos para antibióticos), outras alterações do RNA que não afetem a resistência podem apontar para ideias promissoras para novos antibióticos.
Um desenvolvimento interessante
No corpo humano, um dos papéis mais importantes das proteínas é o controlo do desenvolvimento embrionário. Ao estudarem mutações que causam malformações bizarras na mosca-da-fruta, os cientistas descobriram um conjunto muito importante de proteínas envolvidas no desenvolvimento.
A mais famosa dessas bizarrias é uma mosca-da-fruta que tem uma pata, em vez de uma antena, a crescer na cabeça (veja a foto). Segundo Thomas C. Kaufman, da Indiana University, em Bloomington, a pata é perfeitamente normal, mas está a crescer no local errado.
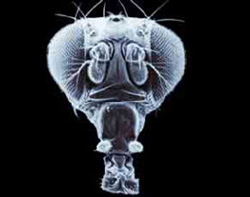
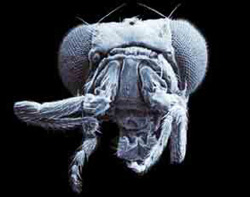
FLYBASE; R. TURNER
Neste tipo de mutação, e em muitas outras, algo corre mal na programação genética que direciona algumas das células do embrião para seguirem vias de desenvolvimento (que são uma série de reações químicas que ocorrem numa ordem específica). No problema da antena-pata, é como se as células que crescem na cabeça da mosca, que normalmente se transformariam numa antena, por equívoco atuem como se estivessem no tórax da mosca e, desse modo, devessem crescer em forma de pata. E assim fazem.
Ao pensar nesta estranha situação, os cientistas aprenderam uma importante lição: as proteínas produzidas por alguns genes podem funcionar como interruptores. Os genes interruptores são controladores mestres que fornecem a cada parte do corpo uma espécie de bilhete de identidade. Se for perturbada uma proteína que levaria a célula a transformar-se numa antena, as células podem receber novas instruções e, em vez disso, transformarem-se numa pata.
Os cientistas determinaram que vários genes diferentes, cada um com uma sequência comum, dão estas instruções de identidade anatómica. Kaufman isolou e descreveu um destes genes, que ficou conhecido como Antennapedia, uma palavra que significa "antena-pata".
Depois, Kaufman começou a estudar com mais detalhe a estrutura molecular do gene Antennapedia. No início da década de 1980, ele e outros investigadores fizeram uma descoberta fundamental para a compreensão da evolução e da biologia do desenvolvimento.
Os cientistas encontraram uma sequência curta de DNA, agora chamada homeobox, que está presente não só no Antennapedia mas em vários genes próximos e em genes de muitos outros organismos. Quando os geneticistas encontram sequências de DNA muito semelhantes em genes de diferentes organismos, essa é uma indicação de que esses genes têm uma função tão importante e útil, que a evolução usa a mesma sequência vezes sem conta e não permite grandes alterações na sua estrutura à medida que as espécies evoluem.
Em pouco tempo, os cientistas descobriram versões quase idênticas do DNA homeobox em quase todas as células não bacterianas analisadas (de leveduras a plantas, rãs, vermes, escaravelhos, galinhas, ratos e humanos).
Foram identificados centenas de genes com homeobox e as proteínas que eles produzem estão envolvidas nos primeiros estádios de desenvolvimento de muitas espécies. Por exemplo, os investigadores descobriram que anomalias nos genes homeobox podem levar ao aparecimento de dedos extra em humanos.
As ferramentas da genética: Os poderosos microarrays
Hoje temos a capacidade de unir um segmento de cada um dos genes do genoma (todos os genes de um organismo) a uma lâmina de microscópio. Esta série ordenada de pontos de DNA é chamada microarray de DNA, chip genético ou chip de DNA.
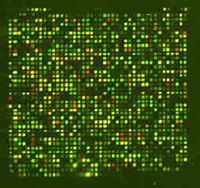
Qualquer que seja o nome que prefiramos usar, o chip também poderia ser apelidado de revolucionário. Esta tecnologia mudou a forma como muitos geneticistas fazem o seu trabalho, ao tornar possível a observação simultânea da atividade de milhares de genes.
Nos últimos anos, os microarrays passaram a fazer parte do equipamento padrão dos biólogos modernos, mas os
professores e alunos também os usam. O programa Genome Consortium for Active Teaching
(www.bio.davidson.edu/GCAT ![]() )
disponibiliza recursos e instruções para que os estudantes do ensino Secundário e Superior possam executar experiências
com chips de DNA na sala de aula.
)
disponibiliza recursos e instruções para que os estudantes do ensino Secundário e Superior possam executar experiências
com chips de DNA na sala de aula.
Os microarrays são utilizados na obtenção de pistas sobre os genes que são expressos para controlar as funções de uma célula, tecido ou órgão. Ao medir o nível de produção de RNA de cada gene simultaneamente, os investigadores podem compreender a programação genética que faz com que os vários tipos de células sejam diferentes e com que as células doentes sejam diferentes das saudáveis.
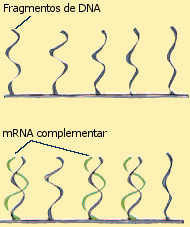
Os chips consistem num grande número de fragmentos de DNA distribuídos em filas num espaço diminuto. As séries (arrays) são distribuídas por robots que conseguem posicionar os fragmentos de DNA de forma tão precisa, que cabem mais de 20 000 numa lâmina de microscópio.

Os cientistas isolam o mRNA de células que cresceram em duas condições distintas e marcam as duas fontes de mRNA com moléculas fluorescentes de diferente cor. Depois, o RNA de duas cores é aplicado ao chip, onde se vai ligar aos fragmentos de DNA complementares, que estão unidos à superfície do chip.
A seguir, um scanner mede a quantidade de fluorescência em cada ponto do chip, revelando quão ativo estava cada gene (quanto RNA produziu cada gene). A análise dos padrões de atividade genética é feita por computador, obtendo-se uma imagem do genoma em duas condições diferentes (por exemplo: saudável e doente).
Em dezembro de 2004, a Agência Americana do Medicamento (Food and Drug Administration) autorizou o primeiro chip de DNA para uso médico. O Amplichip CYP450™, fabricado pela Roche Molecular Systems Inc., de Pleasanton, Califórnia, analisa as variações em dois genes que têm um papel crucial no processamento de muitos medicamentos comuns pelo nosso corpo. Esta informação pode ajudar os médicos a escolher a dose mais adequada de certos medicamentos para um paciente específico.
Compreendeste?
Porque é que algumas infeções são difíceis de tratar com antibióticos? Que passos os investigadores podem tomar para resolver este problema de saúde pública?
De que modo é que o DNA funciona como um meio de armazenamento de informação?
Como é possível que os 20 000 genes humanos possam dar instruções para o fabrico de centenas de milhares de proteínas diferentes?
Qual é o teste de rotina que é feito aos recém-nascidos no hospital da tua zona?


