A Nova Genética
Capítulo 4: Nós somos genes
Para a ciência, a sequenciação do genoma humano foi um feito pioneiro e que teve muita cobertura mediática. Mas o que é que isto realmente significa? Será que esta informação vai fazer alguma diferença nas nossas vidas?
O genoma é todo o material genético de um indivíduo (ou espécie). O genoma humano difere do genoma do gorila, que difere do genoma do arroz, e por aí fora. E, embora todas as pessoas tenham o "genoma humano", ele não é exatamente o mesmo em todas as pessoas. As variações nas sequências dentro dos nossos genes faz com que o nosso DNA seja diferente do da nossa mãe, do nosso primo, ou de um desconhecido.

Pense no genoma humano como uma longa história que contém cerca de 20 000 palavras (os genes). Com poucas exceções, cada pessoa tem o mesmo número de palavras, mas certas palavras têm grafias ligeiramente diferentes. Nalguns casos, as mudanças na grafia geram palavras com novos significados (genes que codificam proteínas diferentes). Outras alterações de grafia parecem não ter efeito algum, pelo menos não aquelas que os cientistas hoje conhecem e sabem quantificar.
Os investigadores estão a começar a usar o conhecimento adquirido com a sequenciação de genomas para descobrirem as diferenças, ao nível molecular, entre estar saudável e estar doente. E os médicos começam a usar a informação genética para escolherem os tratamentos.
Por exemplo, há um teste diagnóstico que pode procurar diferenças no nível de expressão de um gene específico nas células de cancro de mama e prever se a pessoa vai ou não responder ao medicamento chamado Herceptin®.
As células cancerosas de algumas pessoas que têm cancro de mama, produzem proteínas HER2 em abundância, que são o alvo do Herceptin. Para essas pessoas, este é um medicamento milagroso, porque reduz o risco de retorno do cancro de mama e diminu também as hipóteses de morte pela doença.
Nos pacientes de cancro que não expressam a HER2, o Herceptin não tem efeito. Logo, não deverá ser prescrito. A investigação está avançar rapidamente no desenvolvimento de outros testes genéticos que possam ajudar no diagnóstico e tratamento de uma grande variedade de problemas de saúde, para além do cancro.
A leitura do livro dos genes humanos
Em abril de 2003, investigadores por todo o mundo celebraram um marco e um aniversário. Quase 50 anos depois de James Watson, Francis Crick e Maurice Wilkins revelarem a sua descrição da dupla-hélice de DNA, merecedora do Nobel, os cientistas completaram a sequenciação do genoma humano, uma proeza decisiva para a biologia.

L. BARRY HETHERINGTON
Este dia tardou. Na década de 1980, os geneticistas perceberam que tinham, tanto a necessidade, como a capacidade de chegarem à composição completa do genoma humano. Queriam mapear a localização de todos os genes dos cromossomas e decifrar a sequência completa, letra por letra, dos três mil milhões de nucleótidos do genoma.
Os cientistas argumentavam que, dispondo dessa informação, eventualmente seria possível saber qual o papel exato de cada gene, bem como o modo como os genes contribuem para a saúde e doença nos seres humanos.
Em pouco tempo, milhares de cientistas em laboratórios de todo o mundo entraram em ação. As novas ferramentas e tecnologias que faziam com que o trabalho fosse mais rápido e que ajudavam os investigadores a gerir e analisar a avalanche de dados foram fundamentais para o êxito do projeto.

Embora o Projeto do Genoma Humano esteja completo, mantêm-se esforços de sequenciação com ele relacionados. Um desses esforços, envolve a sequenciação dos genomas de muitas outras espécies (veja a secção Os animais a ajudar as pessoas).
Outro é a sequenciação dos genomas de 2000 pessoas para produzir um mapa de haplótipos detalhado que mostre tanto os padrões comuns como os raros da variação genética. Os investigadores podem relacionar estas variações ao risco de doenças ou a carateres relacionados com a saúde, como as reações individuais a medicamentos ou químicos ambientais.
Receitas individualizadas
Uma das formas como a variação genética afeta a nossa saúde, é afetando o modo como o nosso corpo reage aos medicamentos. A inquietante verdade é que os medicamentos só funcionam como esperado em menos de metade das pessoas que os tomam.
Sendo certo que os fatores ambientais e o estilo de vida são parte da explicação, pode-se atribuir uma boa parte da variação individual na resposta aos medicamentos a variações nos genes que dão origem às proteínas da citocromo P450 (veja a secção Os genes encontram-se com o ambiente). Estas proteínas processam muitos dos medicamentos que tomamos.
Como o conjunto de genes de cada pessoa é um pouco diferente, as proteínas que os genes codificam também são ligeiramente diferentes. Estas diferenças podem afetar o modo como as proteínas da citocromo P450 (e muitos outros tipos de proteínas) reagem aos medicamentos.
Os médicos aperceberam-se disto pela primeira vez na década de 1950, quando alguns pacientes tiveram reações adversas (e até fatais) a um anestésico usado em cirurgia. Experiências subsequentes revelaram que aqueles que tinham reagido mal tinham uma variação genética na enzima que degrada o anestésico após a sua permanência no corpo algum tempo.
As pessoas cujos genes codificavam a variante da enzima não tinham qualquer problema até necesitarem de uma cirurgia com anestesia geral. No bloco operatório, uma normal variação genética humana, de repente, levava a uma crise médica!
Felizmente, este tipo de reação drástica a um anestésico é muito rara. Mas, muitas reações a medicamentos não são assim tão raras. Os investigadores sabem que as variações genéticas podem fazer com que alguns medicamentos comuns tenham perigosos efeitos secundários. Por exemplo, algumas pessoas que tomam o medicamento para cancro do cólon Camptosar® (irinotecan) podem desenvolver diarreias e uma infeção com risco de morte, se tiverem a variante do gene para a proteína que metaboliza o irinotecan.
As variações genéticas também podem fazer com que os medicamentos tenham pouco ou nenhum efeito. Por exemplo, em algumas pessoas, os analgésicos com codeína, como o Dolviran®, não aliviam a dor porque os seus corpos degradam-na de modo inusual.
O uso de informação genética para prever o modo como as pessoas respondem a medicamentos é o campo da farmacogenética. O objectivo deste campo de estudo é personalizar os tratamentos com base nos genes do indivíduo.
Com este tipo de aproximação, cada paciente será tratado de forma diferente, porque os médicos terão as ferramentas moleculares para saber, a priori, qual o medicamento a prescrever e em que quantidade (e se o devem prescrever ou não).
O poder curativo do DNA
A farmacogenética está a avançar rapidamente, visto que os cientistas têm à sua disposição muita informação nova do Projeto do Genoma Humano e novas ferramentas computacionais que ajudam na análise da informação. Uma das doenças para as quais o progresso tem sido rápido é o cancro.
O cancro é muitas vezes tratado com um "coquetel" quimioterapêutico, uma combinação de vários medicamentos diferentes. Cada um dos medicamentos da mistura interage com proteínas diferentes, que controlam o modo como o medicamento funciona e a sua velocidade de metabolização no corpo. Para além disso, cada medicamento pode ter os seus próprios efeitos secundários desagradáveis (e até potencialmente perigosos).
Por estes motivos, tratamentos individualizados de quimioterapia baseados na informação genética podem ter benefícios reais para as pessoas com cancro.
Atualmente, a quimioterapia cura cerca de 80% das crianças diagnosticadas com leucemia linfoblástica aguda, o cancro infantil mais comum. Os restantes 20% têm risco de retorno do cancro.
Mary Relling, uma farmacêutica clínica no St. Jude Children's Research Hospital, em Memphis, Tennessee, descobriu que as variações em dois genes podem prever quais os pacientes com leucemia linfoblástica aguda têm hipótese de cura com a quimioterapia. A sua equipa de investigação também identificou mais de cem genes que são expressos apenas nas células cancerosas e que podem ser usados na previsão da resistência aos medicamentos da quimioterapia.
Diz Relling que, ao ter em conta o perfil genético do paciente e das células cancerosas, os cientistas podem criar tratamentos mais efetivos para a doença.
Outros cientistas farmacogenéticos estão a estudar os efeitos de variantes genéticas na resposta dos pacientes a medicamentos que tratam SIDA, alergias, infeções, asma, doenças cardíacas e muitas outras doenças.
Por exemplo, recentemente identificaram duas variantes genéticas diferentes que têm um papel central na determinação da resposta corporal ao Varfine® (varfarina), um medicamento muito prescrito a pessoas com alto risco de coágulos sanguíneos ou ataques cardíacos. Embora dois milhões de americanos tomem este anticoagulante todos os dias, ele é de difícil administração, porque os efeitos variam muito de pessoa para pessoa, mesmo tomando a mesma dosagem. Tomar a dose certa é essencial, porque a varfarina em excesso pode provocar hemorragias, enquanto que em falta pode permitir a formação de coágulos.
Allan Rettie, um químico da University of Washington, em Seattle, descobriu que a variação genética entre as pessoas influencia a atividade de uma proteína do sangue que é o alvo molecular da varfarina. Ele e outros cientistas estão a tentar traduzir esta descoberta num teste genético que possa ajudar os médicos a prever a dose apropriada de varfarina com base no perfil de DNA de cada paciente.
Os genes podem fazer isso?
Sabia que, para além das características que podemos ver, como a cor do cabelo e o físico, os genes também contribuem para o nosso comportamento? E pode parecer surpreendente que muitos investigadores estejam a responder a questões básicas sobre a genética do comportamento pelo estudo de insetos.

ZACHARY HUANG, HTTP://CYBERBEE.MSU.EDU
Por exemplo, Gene Robinson, um entomólogo da University of Illinois, em UrbanaChampaign, trabalha com abelhas. Robinson diz que, se estudarmos as abelhas no seu ambiente natural de colmeia, rapidamente nos apercebemos que elas são muito sociáveis. De facto, segundo Robinson, as abelhas não conseguem sobreviver sem a estrutura social da sua comunidade dentro da colmeia.
Esta característica faz com que sejam uma espécie perfeita para estudar a genética do comportamento.
O que é particularmente interessante nas abelhas é que, em vez de estarem presas a uma tarefa em particular, elas trocam de tarefas dependendo das necessidades da colmeia. Robinson identificou alguns genes cuja atividade se altera com a mudança de função, o que sugere que o ambiente dos insetos ajuda a moldar a sua expressão genética.
Os investigadores que estão a começar a tentar perceber estas conexões estão a trabalhar num novo campo de investigação, designado por Robinson como sociogenómica.
O que é que isto significa para os seres humanos? Isto reforça o facto de, longe de serem rígidos, os nossos genomas são influenciados tanto pela hereditariedade como pelo ambiente, sendo ajustados e esculpidos pela nossa vida social e pelo que fazemos diariamente.
Causa e efeito
Que mais precisamos de saber sobre o modo como os genes moldam quem somos e em quem nos tornamos?
"Muito," diz Richard Lewontin, de Harvard, que lançou um aviso contra a simplificação excessiva do papel dos genes no livro de 2001, "A Tripla Hélice". O principal argumento de Lewontin é que o contexto tem um enorme papel na determinação do crescimento e desenvolvimento dos organismos e nas doenças que estes contraem. O que determina como vai ser uma pessoa, é uma combinação única de fatores genéticos e ambientais, que interagem de um modo difícil de prever.
Poucos cientistas contrariam esta visão. A expressão de um gene e até a tradução do mRNA em proteína dependem do ambiente. Há poucas doenças, a maioria das quais muito raras, que são causadas apenas e só pela mutação de um gene.
Na maioria dos casos, ter ou não doença depende, não só dos genes, mas de fatores que controlamos, como a dieta, o exercício físico e se somos ou não fumadores.

Ainda faltam muitos anos até que os cientistas possam ter uma ideia clara da linguagem detalhada do nosso DNA e do modo como esta interage com o ambiente em que vivemos. Ainda assim, devemos tentar descobrir o máximo de informação sobre o historial de saúde da nossa família. Será que muitos dos nossos familiares tiveram diabetes? Será que há pessoas que tenham tido cancro ou doenças cardíacas?
Lembre-se que doenças como estas são relativamente comuns, portanto há uma boa probabilidade de que pelo menos um familiar nosso tenha uma delas. Mas, se as doenças cardíacas, diabetes ou certos tipos de cancro forem comuns na família, especialmente se muitos dos nossos familiares tiverem a doença quando são jovens, deveremos falar com o nosso médico sobre os riscos de desenvolvermos a doença.
Em 2005, o Cirurgião Geral dos EUA desenvolveu uma plataforma web para organizar a informação de saúde familiar. Esta
ferramenta foi chamada "O Retrato do Coração da Minha Família" (veja
http://www.hhs.gov/familyhistory ![]() )
e organiza a informação num documento que se pode levar para o médico. A informação pode ajudar o médico a determinar os
riscos em relação a várias doenças.
)
e organiza a informação num documento que se pode levar para o médico. A informação pode ajudar o médico a determinar os
riscos em relação a várias doenças.
Se descobrir que tem um risco superior à média para doenças como o cancro de mama ou doenças cardíacas, pode ser capaz de as prevenir ou atrasar o seu aparecimento, alterando a sua dieta, praticando exercício ou mudando o estilo de vida. Pode também tirar partido de rastreios como as mamografias, colonoscopias, ou testes de glicémia para a diabetes. Os testes de rastreio podem detetar as doenças precocemente, quando o tratamento é quase sempre bem sucedido.
Nós contra eles
Muitos cientistas focam-se nos genes humanos, a maioria dos quais possui correspondentes nos genomas de organismos modelo. Contudo, no caso das infeções causadas por microorganismos, a compreensão das diferenças entre o nosso genoma e os de bactérias, vírus, fungos e parasitas é uma área muito importante da investigação médica.
CENTERS FOR DISEASE CONTROL AND PREVENTION
A maioria dos medicamentos que tomamos para tratar infeções bacterianas e víricas, advém da procura dos por pontos fracos moleculares nestes diminutos organismos. Por exemplo, tal como mencionámos no Capítulo 1, alguns antibióticos matam as bactérias desarmando os seus ribossomas.
Então, porque é que eles não matam também células humanas? Porque os ribossomas humanos e os bacterianos são diferentes. A sequenciação genómica é uma poderosa ferramenta para identificar diferenças que podem ser alvos promis-sores de novos medicamentos.
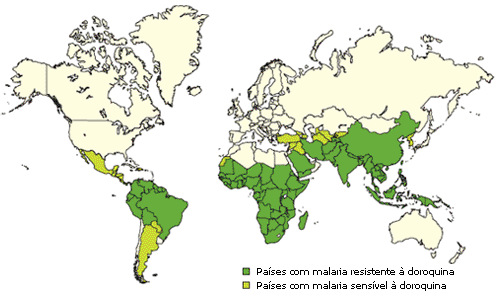
A comparação de sequências genéticas entre organismos resistentes e não-resistentes a medicamentos, pode revelar novas aproximações na luta contra a resistência. Para várias doenças, incluindo a malária, a resistência a medicamentos é um problema mundial.

CDC /JAMES GATHANY
Embora os investigadores tenham desenvolvido diferentes tipos de medicamentos que tratam esta doença – causada por parasitas transportados por mosquitos, e não uma bactéria ou vírus – a malária é agressiva, especialmente nos países em desenvolvimento.
Isto deve-se parcialmente ao facto de nem todas as pessoas terem acesso aos tratamentos ou a medidas simples de prevenção, como as redes mosquiteiras, que protegem as pessoas das picadas de mosquito enquanto dormem. Mas, o próprio parasita da malária é um outro problema, já que evoluiu rapidamente, gerando formas de evitar os efeitos dos medicamentos antimaláricos.
Os cientistas estão a tentar contrariar este processo estudando a informação genética do microorganismo. No caso da malária, geneticistas como Dyann Wirth , da Harvard School of Public Health, comparam os genomas de parasitas resistentes aos medicamentos anti-maláricos com os não resistentes.
A investigação de Wirth sugere que deveria ser possível desenvolver um teste genético, simples e barato, que seria aplicado às pessoas com malária, em qualquer parte do mundo. Este teste identificaria os medicamentos com mais probabilidade de eficácia e ajudaria a diminuir a taxa de aparecimento de resistência dos parasitas aos medicamentos antimaláricos de que já dispomos.
Nós e a genética: Comer menos e viver mais tempo?
Consumiria uma dieta extremamente baixa em calorias se isso significasse viver mais tempo? O tipo de dieta de que falamos não implica só cortar aqui e ali. Envolve uma redução severa na ingestão de calorias para cerca de 60% daquilo que normalmente comemos, o suficiente para que a maioria das pessoas sinta uma fome voraz.

Maurice Gueniot, médico francês do século XIX, pensava que o sacrifício valeria a pena. Ao longo da sua vida adulta, comeu muito pouco. Morreu com uns maduros 102 anos!
Mais tarde, na década de 1930, os investigadores continuaram este tipo de trabalhos e mostraram que ratazanas com uma dieta de 20% de fibra indigerível (calorias que não podem ser usadas) viviam mais tempo que aquelas que recebiam alimento normal.
Intrigados por esta relação da dieta com a saúde, os cientistas continuam a investigar as potenciais conexões entre a dieta e o envelhecimento, e estudos genéticos começam a dar-nos algumas pistas.
Por exemplo, o geneticista David Sinclair, da Harvard Medical School, descobriu que as proteínas conhecidas como sirtuinas podem ser capazes de atrasar o envelhecimento. À medida que as células de levedura vão crescendo, acumulam DNA extra, o que eventualmente as mata. Sinclair descobriu que as sirtuinas ficam mais ativas nas células de levedura que crescem com uma "dieta" baixa em nutrientes. Ele argumenta que, ao limitar a formação de DNA extra, as sirtuinas mantêm as leveduras jovens.
Outros cientistas, como o geneticista Stanley Fields da University of Washington, acham que a conclusão é precipitada. As suas experiências têm indicado que outros genes, não relacionados, estão ligados ao envelhecimento das leveduras. Ele argumenta que, embora a restrição calórica seja a única intervenção que se demonstrou prolongar o período de vida numa ampla gama de organismos (incluindo mamíferos), a acumulação de DNA extra nem sempre parece ter um papel neste processo.
Então, qual é a resposta final? É, prova-velmente, uma mistura de ambas.
Moléculas como as sirtuinas, que estão envolvidas no metabolismo celular, podem proteger as células contra os efeitos nocivos do stress, prolongando o seu período de vida. Outras moléculas, que afetam aspetos diferentes da saúde celular, podem ser igualmente importantes.
O período de vida de organismos multicelulares complexos, como os seres humanos, é afetado por muitos fatores diferentes, acerca dos quais sabemos muito pouco. Com certeza que uma maior compreensão destas moléculas mistério poderia ter um benefício considerável &ndas; quiçá a hipótese de acrescentar anos à nossa vida sem a necessidade de passarmos fome!
Guerra de bandos
Sabia que os cientistas estão a usar a genética para desfazer bandos de...micróbios? Estes bandos, conhecidos como biofilmes, são camadas de "muco" que se desenvolvem naturalmente quando as bactérias se agregam em superfícies como rochas, metal e madeira...ou nos nossos dentes!
P. SINGH E E. PETER GREENBERG
Os biofilmes crescem em todo o tipo de condições. Por exemplo, um biofilme conhecido como "verniz do deserto" cresce em rochas, paredes de desfiladeiros ou, por vezes, em serras inteiras, deixando manchas avermelhadas ou de outras cores. Pensa-se que os petróglifos deixados em rochedos e paredes de cavernas por primitivos habitantes do deserto seriam criados pela raspagem de formações de verniz do deserto com um objeto duro.
Por vezes, os biofilmes têm funções úteis. Um dos melhores exemplos do uso de biofilmes na resolução de problemas importantes, é a limpeza de esgotos.
Mas, os biofilmes podem ser bastante nocivos, contribuindo para uma ampla gama de problemas graves de saúde, como cólera, tuberculose, fibrose quística e intoxicações alimentares. Também estão na base de muitas doenças que não são graves, mas ainda assim problemáticas, como otites e a degradação dos dentes.

DENISE APPLEWHITE
As bactérias formam biofilmes como medida de sobrevivência. Ao viverem em grandes grupos, em vez de isolados, os organismos são capazes de partilhar nutrientes e conservar energia. Como é que fazem isso?
Um biofilme não é só um agregado de células – é uma estrutura altamente sofisticada. Como em qualquer comunidade, os indivíduos do biofilme comunicam entre si.
Porém, muitos aspetos dos biofilmes ainda são mal compreendidos. A geneticista Bonnie Bassler, da Princeton University, em New Jersey, está a trabalhar para uma melhor compreensão dos biofilmes, com o objetivo de ser capaz de usar este conhecimento para desagregar "encontros de bandos" bacterianos.
Os objetos de estudo de Bassler têm um grande apelo visual. Eles brilham no escuro, mas só quando fazem parte de um grupo. A bioluminescência (assim se chama ao brilho) é devida a reações químicas que ocorrem no biofilme. É uma forma das bactérias comunicarem, de estimarem o tamanho da comunidade e de se distinguirem de outros tipos de microorganismos.
Através dos seus estudos, Bassler identificou um conjunto de moléculas que os microorganismos dos biofilmes usam para passarem mensagens entre eles. Bassler argumenta que, desenvolvendo métodos genéticos para cortar a "tagarelice", será capaz de fazer com que as comunidades bacterianas se desagreguem. Esta aproximação seria uma via completamente nova de tratar problemas de saúde associados a biofilmes nocivos.
As ferramentas da genética: Matemática e a Medicina
E se os técnicos de saúde pública tivessem um guião com instruções a seguir no caso de surto de uma doença infecciosa desconhecida? O que os ajudaria na preparação deste tipo de cenário seria a capacidade de saberem, previamente, como é que uma epidemia se desenvolve e alastra.
Com este objetivo em vista, alguns cientistas estão a usar ferramentas matemáticas para criarem simulações, ou modelos, de surtos de doenças infecciosas. Podem depois usar o modelo para testar os efeitos de várias estratégias de intervenção. Parte do trabalho envolve a introdução de informação genética sobre a evolução dos organismos infecciosos ao longo do tempo e da velocidade com que mudam, à medida que interagem com as populações humanas.
Desde 2005, o Models of Infectious Disease Agent Study (MIDAS – Estudo de Modelos de Agentes de Doenças Infecciosas), uma equipa de biólogos, cientistas computacionais, estatísticos, matemáticos, sociólogos e outros, tem estado a modelizar uma pandemia de gripe (uma enorme epidemia global).
Inicialmente, os modelos focaram-se na gripe aviária, um tipo de doença que ocorre, de forma natural, em aves selvagens. Na altura, os especialistas em saúde de todo o mundo estavam preocupados com a possibilidade de mutação do material genético do vírus, o que facilitaria a transmissão desta gripe entre seres humanos.
Para simular a expansão potencial da doença, os cientistas criaram um programa de computador que incorporava informação sobre o vírus da gripe aviária em comunidades reais. A inclusão de detalhes sobre as pessoas (não só as suas idades e sexo, mas também local de residência, trabalho e escola), permitiu aos cientistas criarem uma população sintética que espelhava o modo como uma população real poderia ficar doente e espalhar a doença.

Os cientistas correram os programas em grandes computadores para verem como é que a gripe alastraria, com ou sem diferentes intervenções. Os resultados indicaram que, para controlar a epidemia com êxito, os técnicos de saúde teriam de ser céleres na deteção dos primeiros casos de gripe e implementarem uma combinação de medidas de saúde pública muito rapidamente.
Estes primeiros trabalhos ajudaram os cientistas do MIDAS a desenvolverem modelos semelhantes para o vírus da gripe H1N1, a primeira estirpe de gripe pandémica desde 1968. A partir de abril de 2009, começaram a reunir os dados de saúde pública para simularem a expansão potencial desta gripe global, identificarem os grupos mais propensos a ficarem doentes e avaliarem a utilidade de diferentes medidas de saúde pública, como a vacinação e a quarentena. Os modelos sugeriram que a vacinação das crianças em idade escolar no início de um surto poderia reduzir a expansão da doença, e que as pessoas com risco de complicações graves deveriam tomar medicamentos antivíricos aos primeiros sinais da doença.
Durante os esforços de modelização, tanto da gripe aviária como da H1N1, os cientistas do MIDAS trabalharam em proximidade com os técnicos de saúde pública, para obterem respostas a questões específicas. As respostas foram usadas na elaboração do plano americano para enfrentar pandemias de gripe.
No entanto, a gripe não é a única doença infecciosa que afeta as pessoas. Os cientistas do MIDAS estão também a modelizar outras grandes ameaças à saúde, incluindo a cólera, a febre de dengue, a malária, a tuberculose e a Staphylococcus aureus resistente à meticilina (MRSA).
Compreendeste?
Discute o modo como a matemática pode ajudar os cientistas a colocarem questões sobre a saúde humana.
Contribuirias com uma amostra do teu DNA para a investigação genética sobre doenças comuns, como as doenças cardíaca, depressões ou cancro, mesmo que não tivesses nenhum destes problemas de saúde? Porquê?
Os medicamentos funcionam do modo previsto apenas em metade das pessoas que os tomam. Portanto, os cientistas estão a tentar fazer "medicamentos personalizados", que funcionam muito bem num indivíduo porque correspondem ao seu perfil genético. O desenvolvimento deste tipo de medicamentos levanta algum tipo de problema económico, social ou de outro tipo?


